Últimas noticias sobre el linfoma anaplásico de células grandes asociado a implantes mamarios
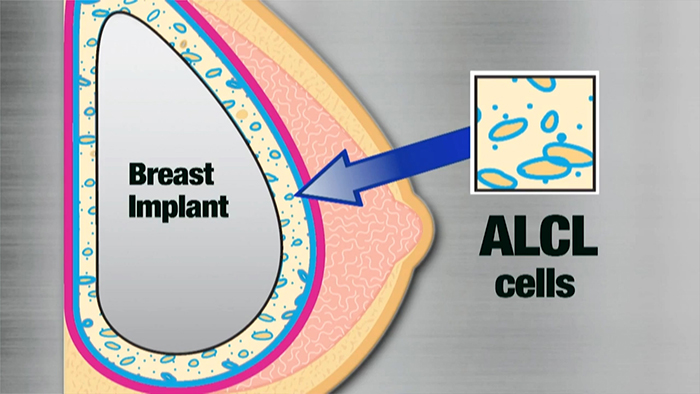
El linfoma anaplásico de células grandes asociado a implantes mamarios (BIA-ALCL, por sus siglas en inglés) es un tipo de linfoma poco común y altamente tratable que puede desarrollarse alrededor de los implantes mamarios. BIA-ALCL ocurre con mayor frecuencia en pacientes que tienen implantes mamarios con superficies texturizadas. El riesgo de vida actual de BIA-ALCL se estima en 1: 3817 - 1: 30,000 mujeres con implantes texturados basados en casos confirmados actuales y datos de ventas de implantes texturados en las últimas dos décadas. Desde el informe inicial del caso en 1996, ASPS ahora reconoce aproximadamente 274 casos en los EE. UU. Y un total de 694 en todo el mundo desde el 19 de abril de 2019.
La mayoría de los pacientes que han desarrollado BIA-ALCL reciben un excelente pronóstico después de la extracción quirúrgica de los implantes mamarios y la cápsula de tejido cicatricial circundante. Se sugiere un seguimiento continuo después de cualquier cirugía de implantes mamarios, que es importante para la salud del paciente, pero los pacientes que noten dolor, bultos, hinchazón, acumulación de líquido o cambios inesperados en la forma de los senos, incluida la asimetría, deben comunicarse con su cirujano plástico. En la mayoría de los casos, las mujeres diagnosticadas con BIA-ALCL observaron cambios en el aspecto o la sensación del área que rodea el implante más de un año después de que los sitios quirúrgicos iniciales se curaron completamente, y en promedio de ocho a diez años después de recibir los implantes texturizados.
Los pacientes que se someten a procedimientos de cirugía plástica, estéticos o reconstructivos, deben estar bien informados sobre los riesgos potenciales y las posibles complicaciones que se sabe que están asociadas con el procedimiento, y cualquier dispositivo utilizado en ese procedimiento. En los casos muy raros en los que se hace un diagnóstico de BIA-ALCL, el tratamiento quirúrgico es esencial para el tratamiento de la enfermedad. Algunos pacientes con enfermedad más avanzada pueden requerir tratamiento adicional como la quimioterapia.
Actualizaciones de la FDA en BIA-ALCL
La actualización del sitio web de la FDA del 6 de febrero de 2019 reconoce que si bien sigue siendo difícil determinar el número exacto de casos de BIA-ALCL, ahora se han reportado 660 informes de dispositivos médicos (MDR) a la base de datos de experiencia de dispositivos de la instalación del usuario y fabricante de la FDA (MAUDE) al 30 de septiembre de 2018, y luego de una revisión exhaustiva, la FDA informa 457 casos únicos que cumplen con los criterios de patología para BIA-ALCL. De estos MDR, los datos incluidos relacionados con la superficie del implante, con 24 identificados como lisos, la mayoría de ellos demuestran una historia clínica de un dispositivo texturizado en la historia clínica. La actualización también confirma que se han informado implantes de gel de silicona y solución salina en casos de BIA-ALCL.
Es importante tener en cuenta que la FDA reconoce que la base de datos MAUDE puede contener informes de eventos adversos limitados y potencialmente inexactos, y puede que no represente el número real de casos en los EE. UU., Ya que algunas entradas son duplicadas y no todos los casos se confirman como ALCL. Aunque la FDA indicó que ha recibido 24 informes asociados con implantes lisos, incluidos algunos casos de BIA-ALCL informados sin problemas, reconocen que esta información no está "verificada" y es potencialmente "inexacta". Hasta el 19 de abril de 2019, 274 casos sospechosos / confirmados de BIA-ALCL en los EE. UU. Se han notificado al registro de pacientes y resultados de los implantes mamarios y el registro de etiología y epidemiología del linfoma anaplásico de células grandes (PERFIL), una colaboración conjunta entre ASPS, PSF y La FDA.
La actualización del sitio web de la FDA confirma las comunicaciones de ASPS anteriores, y señala que BIA-ALCL sigue siendo una condición rara que ocurre con más frecuencia en pacientes que tienen implantes mamarios con superficies texturadas. El informe también reitera que los pacientes deben hablar con su proveedor de atención médica sobre los beneficios y riesgos de los implantes de superficie texturada frente a los de superficie lisa. La FDA destaca el reconocimiento de BIA-ALCL de la Organización Mundial de la Salud y las pautas estandarizadas de diagnóstico y tratamiento establecidas por la Red Nacional de Cáncer Integral (NCCN, por sus siglas en inglés).
La FDA recomienda que todos los casos de BIA-ALCL se informen a la FDA y al registro de PERFIL.
Para obtener más información sobre BIA-ALCL, visite plasticsurgery.org/alcl o el sitio web de la FDA.
Nuestra práctica está comprometida con la seguridad del paciente, la mejora de la calidad de la atención y la práctica de la medicina basada en la mejor evidencia científica disponible. Continuaremos monitoreando y revisando toda la información nueva a medida que esté disponible para mantener informada a la comunidad de cirugía plástica.
Fuente: Sociedad Americana de Cirugía Plástica.

